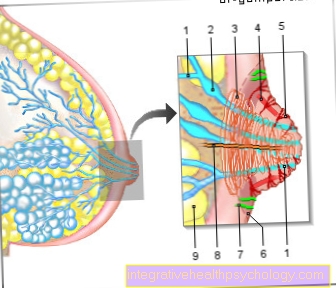
ペンタロン®
有効成分:ペンタエリスリチル四硝酸塩
作用機序

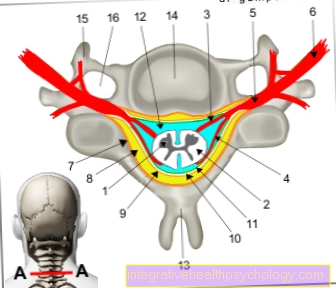
有効成分は血管拡張物質のグループに属します(硝酸塩)そして狭窄した冠状動脈の場合に心臓への血流を促進するために使用されます。
生物では、有効成分は身体自身の一酸化窒素になります(番号) 削減。これは、船に直接拡大効果をもたらします。
血液循環の改善により、心臓への酸素供給が改善され、胸痛(狭心症)の発作が防止されます。
硝酸塩のグループの他の薬剤とは対照的に、Pentalong®は、硝酸塩に関連した頭痛や耐性の発達につながるべきではありません。
ペンタロン®は、以前は80mgと50mgの用量で販売されていました。しかし、2014年5月20日以来、狭心症の患者における高用量の十分な効果が十分な研究で示されていないため、この薬剤は50 mgの用量でのみ承認されています。
薬は処方箋でのみ利用可能です。予防や長期治療に適しています。
摂取
患者は別段の定めがない限り服用します 1日2〜3錠 ペンタロン®50mg丸1食前約30分。
治療担当医師は、治療期間または別の摂取量を決定します。
過剰摂取が疑われる場合は、治療を中止し、直ちに医師の診察を受けてください。
錠剤を忘れてしまった場合は、2回服用せずに、次の定期的な摂取時間に投薬を続けてください。
副作用
患者は非常に一般的な副作用として不満を訴えます(10人の患者に1人以上が治療されます) 頭痛.
頻繁に(100人中1〜10人の患者)、以下のような望ましくない症状を引き起こす可能性もあります 低血圧, 循環調節障害 と 崩壊, めまい, 眠気 そして 速いハートビート 来る。
ときどき(1,000人中1〜10人のユーザーに影響します)、発生します 皮膚の一時的な発赤 (流す)および アレルギー性皮膚反応.
発生頻度が少ない(10,000人に1〜10人のユーザー) 吐き気 そして 嘔吐, 皮膚の発疹, 心不整脈 または 呼吸困難 オン。
Pentalong®を服用した結果、非常にまれ(10,000人に1人未満)が観察されました 重度の炎症性皮膚疾患 (例えば、剥脱性皮膚炎、スティーブンス-ジョンソン症候群、血管性浮腫)。
これらまたは他の症状に気づいたらすぐに医師に通知するか相談し、薬を再度服用しないでください。
相互作用
Pentalong®に加えて他の薬を服用するときは、 薬の効果 それによって おそらく強化 することができます。これは、例えば、同時に取ることに適用されます ベータ遮断薬, カルシウムチャネル遮断薬, 利尿薬, ACE阻害剤, ホスホジエステラーゼ阻害剤、確かな 抗うつ薬 そして 神経遮断薬、および アルコール消費量.
ペンタロン®はまた、 弱体化 の効果 ヘパリン製剤.
対照的に、グループの準備 麦角アルカロイド (例:ジヒドロエルゴタミン)ペンタロン®を服用すると増加 高血圧.
禁忌
Pentalong®は、 有効成分に対するアレルギー/不耐性, 急性心血管障害, ショック, 心臓発作, 非常に低い血圧 (収縮期値<90mmHg)、および 並行摂取 から ホスホジエステラーゼ阻害剤 勃起不全の治療のため(例えば シルデナフィル, バルデナフィル, タダラフィル)、これにより血圧が著しく低下する可能性があります。
他の特定の状況では、医師はPentalong®を服用しても安全かどうかを注意深く確認する必要があります。だから例えば。で 頭蓋内圧の上昇 そして多数 心臓病 (心筋炎心臓弁の収縮、心筋の肥厚、心筋の顕著な衰弱、心膜への体液の蓄積)。
妊娠中および授乳中の使用
の中に 妊娠 そして 授乳 薬は 取られない、この間、アプリケーションが安全であるかどうかについてはまだ十分な知識がないため。
子供および青年での使用
現在、Pentalong®の子供および青年期における安全性に関する知識は不十分です。したがって、薬は若者に使用されます 必要性を注意深く検討して初めて 使用する。
警告
ペンタロン®を服用すると、 反応性限定 あります。
したがって、道路交通に参加するとき、または 機械を操作する 最高の 注意 必須。これが当てはまる 特に治療開始時、 線量増加 と関連 アルコール消費量.
薬は 治療のためにも 1 急性狭心症, まだ 治療する 急性心臓発作 適切。
Pentalong®も含まれています 乳糖 (乳糖)、対応する不耐性を持つ人々はアレルギー反応を起こす可能性があります。
バックグラウンド
発展した でペンタロン®になりました 1950年代のアメリカ.
1964年以来、それはツヴィッカウからの会社によって旧東ドイツで生産されました。
今日は Actavisの権利 Pentalong®。
薬は決して承認プロセスを経る必要がなかったので、アクタビスはその後の承認を申請しなければなりませんでした。これは、品質、有効性、安全性をチェックする必要があったため、1976年以前に上市されたすべての医薬品の手順でした。
ただし、Actavisは連邦医薬品医療機器研究所によって設定された要件を満たしていないため、 の入場 ペンタロン® 2005年に期限切れ.
Actavisはこの決定を訴え、その後、Pentalong®80mgの有効性を証明するはずの研究を提出しました。研究は説得力がなかったので、 この薬の承認は2014年にようやく終了しました.
のために 50mgでより少ない投与量 まだ存在しています 架空の入場この薬が市場性を維持できるように。
ただし、 法定健康保険で償還されなくなった。患者は自己負担しなければなりません。
したがって、多くの患者で 切り替え ペンタロン®の薬 硝酸塩を含む他の薬に 実行されました。代替有効成分は、例えば 硝酸イソソルビド (ISDN)および 一硝酸イソソルビド (ISMN)、および必要に応じて ニトロスプレーこれも硝酸塩のグループに属しているため、血管拡張効果があります。











.jpg)
.jpg)